燃料電池
燃料電池とは?
燃料電池とは、水素と酸素による電気化学反応により電力を取り出し発電させる装置です。発電の際に排出されるのは水だけなので、クリーンエネルギーとし て注目されています。また、発電効率が高く、小型化が容易なため、燃料電池車など、多岐にわたる応用が期待されています。
燃料電池のアイデアは、19世紀の初めにイギリスのDavyによって提唱されたと言われていますが、デモンストレーション実験は1839年、イギリスの Groveによって行われました。その後、1965年にはアメリカの人工衛星Gemini5号の電源として、出力1kWの燃料電池が搭載されました。当時 は宇宙用や軍事用を目的に開発が進められていましたが、90年代には燃料電池を動力源として搭載した燃料電池車が登場し、現在では多くの研究者が実用化に 向けて研究を行っています。
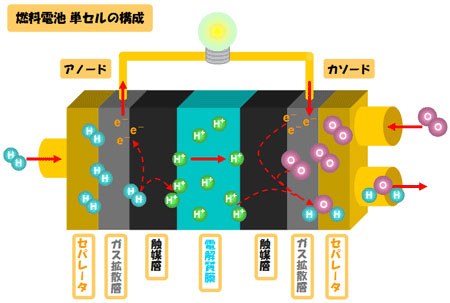
燃料電池の単セルは、電解質膜、およびその両側に触媒層、ガス拡散層、さらにその外側にあるセパレータによって構成されています。
アノードには外部から水素ガスが供給され、ガス拡散層を通って触媒層に達すると、白金触媒の表面で水素分子(H2)は水素イオン(H+)と電子(e)にわかれます。
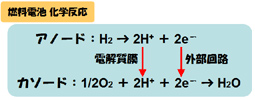 水素イオンは電解質膜を通ってカソード側へ移動し、電子は外部回路を通ってカソードに到達します。そしてこの電流が外部に電力として取り出されます。一方 カソードには外部から酸素ガスが供給され、外部回路を経て到達した電子(e)と、電解質中を移動してきた水素イオン(H+)が触媒上で反応して水となりま す。 水素イオンは電解質膜を通ってカソード側へ移動し、電子は外部回路を通ってカソードに到達します。そしてこの電流が外部に電力として取り出されます。一方 カソードには外部から酸素ガスが供給され、外部回路を経て到達した電子(e)と、電解質中を移動してきた水素イオン(H+)が触媒上で反応して水となりま す。 |
この単セルは、理論的な起電力が1.23V、出力を取り出した時の電圧は1V以下と低電圧の直流電源です。家庭用電源や燃料電池車などの実用的な電圧を得るためには、単セルを数百個直列に接続したスタックセルが用いられます。
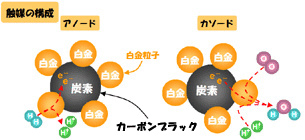 また反応に直接関与している触媒層は主に触媒担体である炭素と白金粒子から構成されています。現在では主に触媒担体炭素としてカーボンブラックが用いら れていますが、実用化に向けた課題の1つとして、この触媒担体炭素の劣化が挙げられます。また、触媒担体炭素の比表面積は、それに担持する白金の粒子サイズと分布状態にも影響を与えます。そのため、比表面積のより大きい材料の触媒担体への応用が望まれています。 また反応に直接関与している触媒層は主に触媒担体である炭素と白金粒子から構成されています。現在では主に触媒担体炭素としてカーボンブラックが用いら れていますが、実用化に向けた課題の1つとして、この触媒担体炭素の劣化が挙げられます。また、触媒担体炭素の比表面積は、それに担持する白金の粒子サイズと分布状態にも影響を与えます。そのため、比表面積のより大きい材料の触媒担体への応用が望まれています。 |
当研究室では、これまでにカーボンナノチューブ、カーボンナノウォール、フラーレンナノウィスカーなど様々な炭素材料を創製してきました。これらの材料 は化学的に非常に安定であり、電極材料への応用が期待されています。当研究室ではこれらの新規炭素材料を電極材料として燃料電池を作製し、I-V特性曲線 やX線回折(XRD)、ラマン分光法などの他様々な測定方法を用い、その評価を行っています。